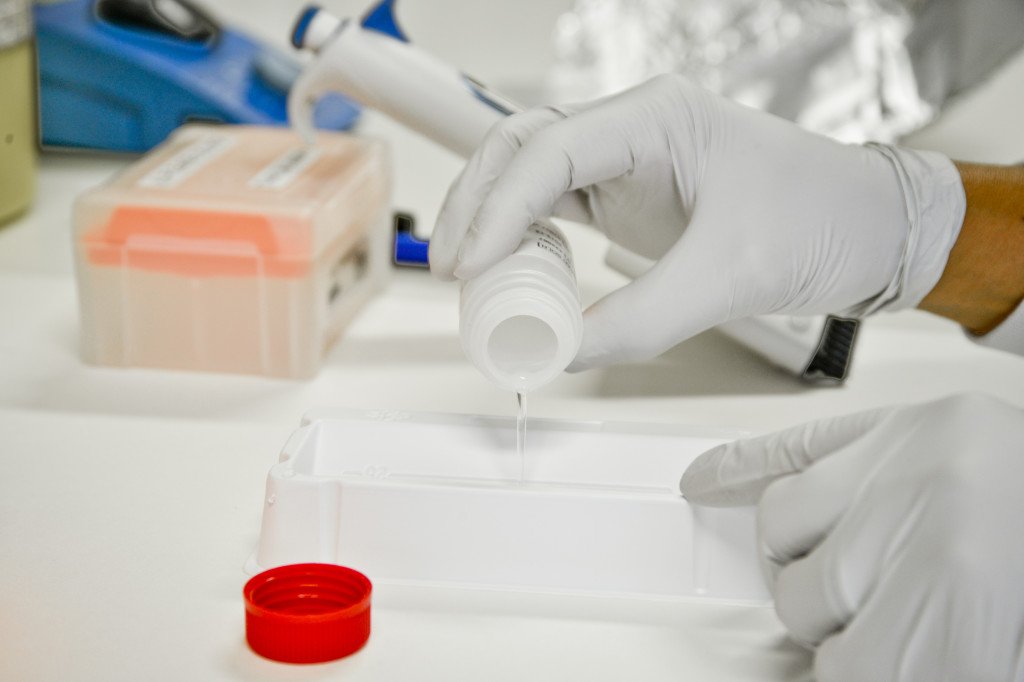
Aziende farmaceutiche e ricercatori universitari dovranno pubblicare i risultati di tutte le sperimentazioni
Fra le normative approvate nei giorni scorsi dal Parlamento europeo spicca quella in campo medico, che facilita la cooperazione transnazionale per condurre test clinici su larga scala così da incrementare, a sua volta, gli sforzi per sviluppare trattamenti speciali, ad esempio per le malattie rare.
L’atto legislativo snellirà le norme in materia di test clinici in tutta Europa, consentendo test più affidabili, perché faciliterà la procedura di comunicazione e autorizzerà la Commissione europea a fare controlli. Una volta che uno sponsor di test clinici presenterà un dossier di domanda, lo Stato membro dovrà rispondere entro i termini stabiliti.
Per la relatrice del testo Glenis Willmott, laburista inglese (gruppo Alleanza progressista di Socialisti e Democratici) «i test saranno effettuati in maniera più trasparente, dando maggiore speranza ai pazienti che necessitano nuovi e migliori trattamenti, aumentando il numero di posti di lavoro qualificati e di ricerca in Europa. Questo semplicemente perché non c’erano abbastanza pazienti in un solo Paese per sviluppare o migliorare nuovi trattamenti alle malattie rare, ora invece potremo ridurre l’enorme costo e l’onere di condurre test al di la delle frontiere».
I parlamentari europei hanno modificato il progetto legislativo per migliorare la trasparenza, richiedendo che riassunti dettagliati siano pubblicati in una banca dati europea accessibile al pubblico, includendo tutte le relazioni di studi clinici che saranno pubblicati una volta che sarà presa una decisione in merito all’immissione sul mercato o che la domanda di autorizzazione sarà respinta.
Fiasha Van Dijk
© 2014 European Parliament